
一、产品介绍
|
外观: |
白色无定形粉末。 |
|
冻干缓冲液: |
50mM PB-K,1mg/ml BSA,pH7.0 |
|
比 活 力: |
≥70U/mg干粉(乳酸底物法);≥100U/mg干粉(丙酮酸底物法)。 |
|
稳 定 性: |
干粉于-20℃至少稳定一年。 |
|
分 子 量: |
~38kD (SDS-PAGE) |
|
等 电 点: |
7.89 |
|
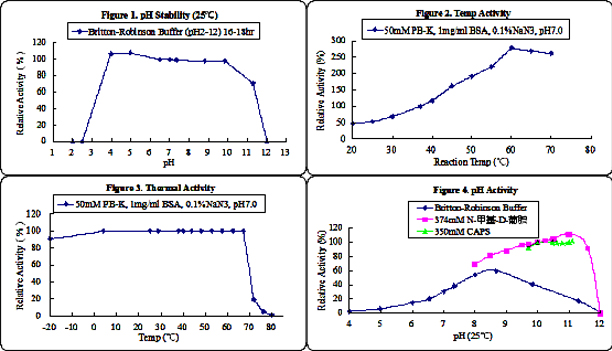
pH稳定性 : |
4.0~10.0稳定 (500-1000U/L,25℃,24hr) (Figure 1) |
|
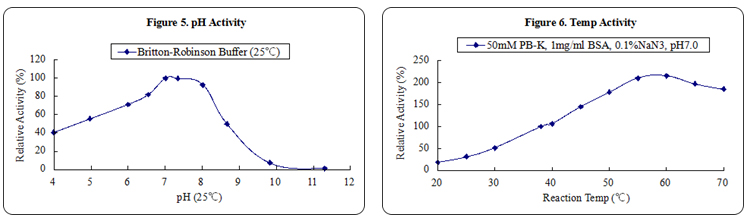
最 适pH : |
10.0-11.0 (乳酸底物法, Figure 4);7.0~8.0 (丙酮酸底物法, Figure 5) |
|
最适温度 : |
60℃ (Figure 2 and 6) |
|
热稳定性 : |
1kU/L时60℃加热30min不失活(乳酸底物法)。 (Figure 3) |
|
稳 定 剂: |
添加≥1mg/ml BSA有助于稀释样品的稳定。 |
|
复 溶: |
用去离子水或50mM PB-K (pH 7.0) 复溶。 |
二、乳酸底物法测定酶活
2.1 测定原理
在强碱性条件下,鸡心L-LDH催化L-乳酸与NAD+反应生成丙酮酸和NADH。在一定范围内NADH的生成速率与L-LDH活力成正比。在340nm处测定NADH的生成速率,根据酶活计算公式即可测出酶活力。1个酶活单位(U)等于在下述反应条件下每分钟生成1微摩尔NADH所需的酶量。

2.2 检测方法
1. 酶稀释液:50mM PB-K,1mg/ml BSA,0.1% NaN3,pH7.0。过0.22um滤膜后2-8℃保存,保质期1年。
2. Buffer:350mM CAPS(Mr=221.32),0.1% NaN3,pH10.0 (25℃),过0.22um滤膜后2-8℃保存,保质期一个月。
3. R1:1M 乳酸锂,0.1% NaN3。过0.22um滤膜后2-8℃保存,保质期一个月。
4. R2:9mM NAD ,0.1% NaN3。过0.22um滤膜后2-8℃保存,保质期为一周。
1. R:临用前按Buffer : R1 : R2=920ul : 80ul : 200ul比例混合,2-8℃保存,保质期1天。用前恢复室温。
2. 待测酶液S:称量所需的酶粉,用去离子水或50mM PB-K (pH 7.0)复溶,定容到既定体积配制成待测酶液S。用酶稀释液将其稀释至200-2000U/L内的2-5个梯度。
3. 酶活检测步骤
1) 将1200ul的R添加至“d=1.0cm”的石英比色皿中,37℃温育1min;然后加入20ul待测酶液 S,充分混匀后,37℃反应至3min;记录第2-3min内OD340的变化,并计算每分钟吸光值变化率(△As/min)。测活历程如下:
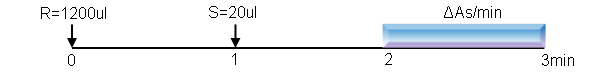
2) 重复以上步骤,用20μl酶稀释液作为阴性对照。记录空白吸光值(△Ab/min)。
1. 计算公式
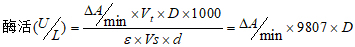

|
Vt |
:反应液总体积(ml) |
|
ε |
:NADH摩尔吸光系数6.22(cm2/micromole) |
|
Vs |
:样品体积(ml) |
|
d |
:比色杯光程(1cm) |
|
D |
:稀释倍数 |
|
△A/min |
:△As/min-△Ab/min |
|
方向 |
:升反应 |
|
线性 |
:0-2000U/L,建议稀释至200-2000U/L。 |
2.3 酶性质附图(乳酸底物法)
三、丙酮酸底物法测定酶活 
3.1 测定原理
在中性偏碱条件下,鸡心L-LDH催化丙酮酸和NADH反应生成L-乳酸与NAD+。在一定范围内NADH的消耗速率与L-LDH活力成正比。在340nm处测定NADH的消耗速率,根据酶活计算公式即可测出酶活力。1个酶活单位(U)等于在下述反应条件下每分钟消耗1微摩尔 NADH所需的酶量。
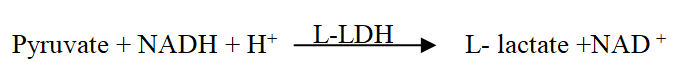
3.1 检测方法
1. Buffer:100mM PB-K,pH7.0。
2. 酶稀释液:50mM PB-K,1mg/ml BSA,0.1%NaN3,pH7.0。过0.22um滤膜后2-8℃保存,保质期1年。
3. R1:100mM PB-K,25.4mM丙酮酸钠盐或钾盐,0.1%NaN3,pH7.0。过0.22um滤膜后2-8℃保存,保质期一个月。
4. R2:10mM Tris-HCl, 10mg/ml NADH,0.1%NaN3,pH9.7,过0.22um滤膜后2-8℃保存,保质期1周。
5. R:临用前按Buffer : R1 : R2=3000ul : 100ul : 50ul比例混合,2-8℃保存,保质期1天。用前恢复室温当OD340<0.8时,重新配置R。若OD340依然小于0.8,请重新配置R2。
6. 待测酶液S:称量所需的酶粉,用去离子水或50mM PB-K (pH 7.0)复溶,定容到既定体积配制成待测酶液S。用酶稀释液将其稀释至500-3000U/L范围内的2-5个梯度。
7. 酶活检测步骤
1) 将1200ul的R添加至“d=1.0cm”的石英比色皿中,37℃温育1min;然后加入20ul待测酶液 S,充分混匀后,37℃反应至3min;记录第2-3min内OD340的变化,并计算每分钟吸光值变化率(△As/min)。测活历程如下:

2) 重复以上步骤,用20μl酶稀释液作为阴性对照。记录空白吸光值(△Ab/min)。
8. 计算公式

|
Vt |
:反应液总体积(ml) |
|
ε |
:NADH摩尔吸光系数6.22(cm2/micromole) |
|
Vs |
:样品体积(ml) |
|
d |
:比色杯光程(1cm) |
|
D |
:稀释倍数 |
|
△A/min |
:△As/min-△Ab/min |
|
方向 |
:降反应 |
|
线性 |
:0-3000U/L,建议稀释至500-3000U/L。 |
3.3 酶性质附图(丙酮酸底物法)
IVD原料


