一、产品介绍
|
外 观: |
白色无定形粉末 |
|
蛋白比活: |
≥20,000 Kunitz units/mg protein |
|
纯 度: |
不含RNase、蛋白酶、其它DNA内切酶和外切酶;≥95%(SDS-PAGE) |
|
稳 定 性: |
-20℃至少稳定2年 |
|
分 子 量: |
~35kD的糖蛋白 |
|
等 电 点: |
6.0左右 |
|
抑 制 剂: |
EDTA 、EGTA、SDS、DTT、β-巯基乙醇等还原剂 |
|
激 活 剂: |
Mg2+,Mn2+,Ca2+,Co2+,Zn2+ |
|
pH稳定性: |
4.0-9.0(25℃,24h) |
|
最适 pH: |
6.0 |
|
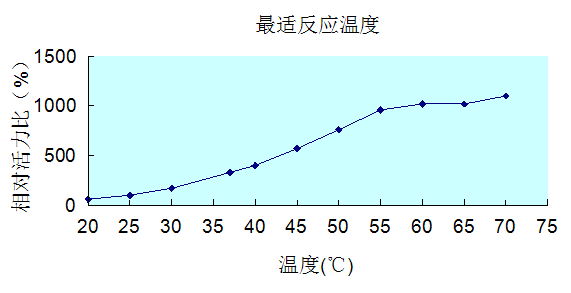
最适温度: |
活力随温度(20℃-60℃)升高逐渐升高;37℃测值为25℃测值的3.3倍。 |
|
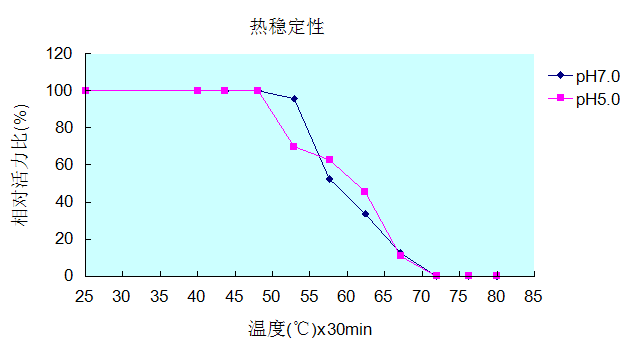
热稳定性: |
55℃以下稳定;60℃加热30min后活力依然保留50%以上;70℃以上失活。 |
二、酶活测定方法
1. 原理
利用DNase降解DNA生成寡核苷酸时260nm处的吸光值会升高的原理,在一定条件下,OD260每分钟的增加率与DNase的含量成正比例。以牛胸腺DNA为底物,在pH5.0、25℃条件下,1Kunitz unit能使OD260每分钟增加0.001。
2. 测活试剂
2.1 1M 醋酸钠缓冲液 (pH 5.0):将13.6g醋酸钠溶于80ml去离子水,再用6M HCl调pH 5.0(25℃),加去离子水定容至100ml,室温保存。
2.2 100mM MgSO4:将1.2g MgSO4溶于100ml去离子水,室温保存。
2.3 0.033% (W/V)小牛胸腺DNA
1)将100mg 小牛胸腺DNA(欣经科 货号:7026)溶于300ml预冷的去离子水中,冰浴至少30min,缓慢搅拌至完全溶解。分装后,冻存于-20℃。临用前在37℃解冻。
2)测定DNA的浓度
a. 用去离子水将1.1.3底物DNA样品稀释N倍(10-30倍),以去离子水作为阴性对照。
b. 用UV分光光度仪测定OD260,以阴性对照归零。
c. 1个OD260单位相当于50μg/ml DNA,DNA浓度的计算公式如(1.1)。
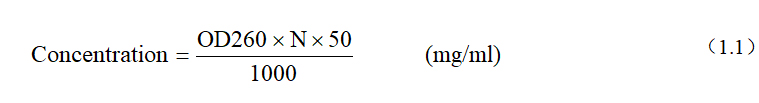
2.4 酶稀释液:即0.85% NaCl(150mM)。将0.85g NaCl溶于100ml去离子水,室温保存。
2.5 反应液R
1)按下表配置50ml 反应液R。
2)轻柔混匀后,用0.1M HCl和0.1M NaOH调pH 5.0 (25ºC)。2-8℃可稳定保存至少2个月。
3)*注意:根据4.3测得的DNA浓度适当添加去离子水和底物DNA。测活试剂R中DNA的终浓度为0.004%(w/v) ,即40ug/ml,OD260吸光值为0.8。
|
试 剂 |
ml |
|
1M 醋酸钠(pH 5.0) |
5.0 |
|
100mM MgSO4 |
2.5 |
|
0.033% (W/V)小牛胸腺DNA |
6.0* (2.0mg of DNA) |
|
去离子水 |
36.5* |
3. 待测样品的配制
测活前,用酶稀释液溶解重组型bpDNase I干粉后,再用酶稀释液将酶液稀释至200-500 Kuniz units/ml,按以下步骤检测酶活。
4. 酶活检测步骤
在1cm的石英比色杯中加入2.5ml 2.2.2测活试剂R,25℃条件下保温1.5min后,加0.5ml待测样品,迅速混匀,在260nm波长下读取2min内最大的吸光度变化率(ΔA260nm/min Sample)。同时以0.5ml去离子为空白对照,记录ΔA260nm/min Blank。按照以下公式计算酶活力。线性范围是400-500U/ml。3.00ml反应体系含83mM 醋酸钠缓冲液(pH5.0),4.2mM MgSO4,25mM NaCl,33.33ug/ml小牛胸腺DNA及200-250 Kuniz units DNase I。酶活力计算公式:
Activity(Kunitz Units/ml)= (ΔA260nm/min Sample -ΔA260nm/min Blank) X (3) X D =△A/min×6000×D
0.001×0.5×1
|
Vt |
反应液总体积 (3ml) |
|
ε |
0.001 = ΔA 260nm per the unit definition |
|
Vs |
样品体积 (0.5ml) |
|
d |
比色皿光程 (1cm) |
|
D |
稀释倍数 |
|
△A/min |
△A/min Sample -△A/min Blank(单位:Abs/min) |
三、酶性质
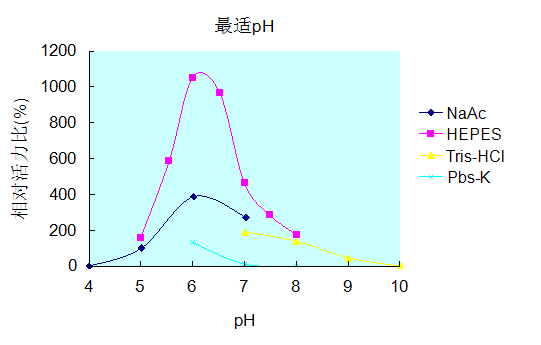
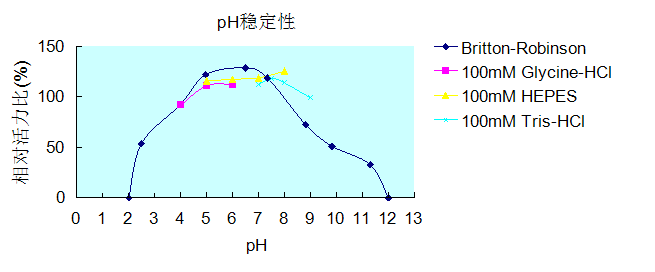
IVD原料


