
一、产品介绍
|
外观: |
白色无定形粉末 |
|
比 活 性: |
≥40U/mg |
|
稳 定 性: |
|
|
分 子 量: |
116.5KD |
|
等 电 点: |
5.28 |
|
米氏常数: |
4.33×10-4M (2-Nitrophenyl-β-D-galactoside) |
|
抑 制 剂: |
不受叠氮钠的抑制 |
|
pH稳定性: |
5.0~9.5 (Fig. 1) |
|
最 适 pH: |
7.5 (Fig. 2) |
|
最适温度: |
55℃ (Fig. 3) |
|
热稳定性: |
|
二、酶活测定方法
1. 检测原理

2. 酶活定义
一个酶活单位等于在检测条件下每分钟转换(水解) 1.0μmol底物(O-硝基酚β-D-半乳糖苷)的酶量。
3. 检测方法
3.1 酶活检测试剂配制方法
3.1.1 试剂A的配制
100mM,pH 7.3的磷酸钠缓冲液。
3.1.2 试剂B的配制
3.36M β-巯基乙醇:将4ml β-巯基乙醇用水稀释至17ml(现配现用)。
3.1.3 试剂C的配制
30mM 氯化镁溶液:将610mg MgCl2·H2O溶于80ml水,使用1M NaOH调pH至7.3,定溶至100ml。
3.1.4 试剂D的配制
22.7mM O-硝基酚β-D-半乳糖苷溶液:将137mg ONPG溶于20ml试剂A(0-5℃可保存1周)。
3.1.1 试剂E的配制
测活试剂:将试剂A,试剂B,试剂C按照8:1:1的比例混合。
3.1.2 试剂F(酶稀释液)的配制
酶稀释液:50mM pH7.3的磷酸钠缓冲液,含1.0mM MgCl2,0.1% BSA。
3.1 待测样品的配制
检测前用卧氏称量管称量所需酶,酶称量时,应至少称量10毫克的酶,以保证称量的准确性。用酶稀释液溶解,定容到配制体积,室温放置1小时。测定前使用酶稀释液(F)稀释至100-1000U/L。
3.2 酶活检测步骤
1、0.520ml试剂E与0.02ml稀释好的酶液在
2、加入0.06ml试剂D,37℃反应4分钟。记录吸光值,计算第3分钟到第4分钟的单位时间吸光度变化(△OD405/min (test))。
3、重复第1、2步骤,用20微升的酶稀释液代替酶液。计算单位时间吸光值变化(△OD405/min (blank))。
注意:此法酶的最适线性为100-1000 U /L。
3.3 酶活力计算公式
酶活力(U/L)= 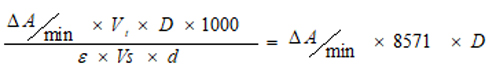
酶比活力(U/mg)= 
|
△A/min |
:△OD405/min(test)- △OD405/min(blank) |
|
Vt |
:反应液的总体积(0.6 ml) |
|
D |
:稀释倍数 |
|
ε |
:生成的ONP在405nm的消光系数3.5 (cm2/μmol) |
|
Vs |
:酶液体积(0.02ml) |
|
d |
:比色杯光径( |
三、 附图

IVD原料


